ROUNDUP 2/Merck: Neuaufnahme von MS-Patienten in USA gestoppt - Kurseinbruch
(neu: weitere Analystenstimme, Zahl der Studienteilnehmer und Aktienkurs)
DARMSTADT (dpa-AFX) - Schlechte Nachrichten für den Darmstädter Pharma- und Technologiekonzern Merck KGaA (Merck KGaA Aktie)
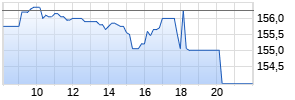
Das Kursniveau markierte den tiefsten Stand seit Oktober 2022. Laut JPMorgan-Analyst Richard Vosser ist mit dem Kursrutsch der Marktwert von Evobrutinib komplett ausgepreist. Er hält die Reaktion der Anleger für "angemessen", da es durch die Bedenken der FDA in Zukunft Probleme bei der Zulassung des Medikaments in den USA geben könne. Dafür spricht seiner Meinung nach auch, dass es beim Pharmakonzern Sanofi
Das von Merck KGaA getestete Mittel soll zur Behandlung für schubförmige Multiple Sklerose (RMS) eingesetzt werden. Schwächere Studienergebnisse könnten Merck auch finanziell durchaus treffen: Analyst Vosser rechnet mit einem maximalen Umsatzpotenzial des Medikaments von 2,4 Milliarden Euro - wovon die Hälfte mit Risiken behaftet sei.
Seine Kollegin Rosie Turner vom Analysehaus Jefferies hatte jüngst in einer Studie das ohne Risiken behaftete maximale Umsatzpotenzial für Evobrutinib auf zwei Milliarden Euro geschätzt. In einem optimistischen Szenario zum Mittel veranschlagte sie den Umsatzbeitrag zum Gesamtumsatz der Pharmasparte von Merck für die Jahre 2025 bis 2030 auf zwei bis vier Prozent.
Laut den von der FDA angeordneten Maßnahmen darf in den USA nun bei neuen Patienten keine Behandlung mehr mit dem Mittel eingeleitet werden, sowie bei jenen, die weniger als 70 Tage mit der Studienmedikation behandelt wurden. Da alle Studienteilnehmer aber schon länger als 70 Tage behandelt werden, wird die Therapie laut Merck fortgeführt. "Für uns ändert sich nichts", sagte ein Merck-Sprecher auf Nachfrage.
Die auf Leberschäden hinweisenden Laborwerte von zwei Patienten wurden während einer Phase-III-Studie festgestellt. Beide Personen seien aber asymptomatisch gewesen und brauchten weder eine medizinische Intervention noch stationäre Behandlung, teilte Merck weiter mit. Nach Absetzen des Medikaments hätten sich die Leber-Werte zudem vollständig normalisiert. Die Darmstädter versicherten, mit der US-Behörde zusammenzuarbeiten, um das weitere Vorgehen in laufenden und zukünftigen Studien zu Evobrutinib festzulegen. Derzeit gäbe es 2 000 Patienten in Phase III der Studie./lew/niw/jha/
Mehr Nachrichten zur Merck KGaA Aktie kostenlos abonnieren
(Mit der Bestellung akzeptierst du die Datenschutzhinweise)

Hinweis: ARIVA.DE veröffentlicht in dieser Rubrik Analysen, Kolumnen und Nachrichten aus verschiedenen Quellen. Die ARIVA.DE AG ist nicht verantwortlich für Inhalte, die erkennbar von Dritten in den „News“-Bereich dieser Webseite eingestellt worden sind, und macht sich diese nicht zu Eigen. Diese Inhalte sind insbesondere durch eine entsprechende „von“-Kennzeichnung unterhalb der Artikelüberschrift und/oder durch den Link „Um den vollständigen Artikel zu lesen, klicken Sie bitte hier.“ erkennbar; verantwortlich für diese Inhalte ist allein der genannte Dritte.